[열역학 1] 계와 기본용어 등
1.동작물질과 계
1.1.동작물질 : 열기관에서 열을 일로 혹은 일을 열로 전환하는데 필요한 매게물질 // 작동물질
1.2.계 (system) : 열역학에서 대상으로 하는 이들 물질의 한정된 공간
1)개방계 : 계의 경계를 통해서 에너지와 물질 모두가 출입 가능한 계 // 열린계
2)밀폐계 : 계의 경계를 통해서 에너지는 출입가능하나 물질은 출입 불가능한 계
3)절연계 : 계의 경계를 통해서 에너지와 물질 모두가 출입 불가능한 계 // 닫힌계, 고립계
1.3.주위와 경계
1)주위 : 계가 아닌 계주위의 부분
2)경계 : 계와 주위를 구분짓는 한계
1.4.정상류와 비정상류
1)정상류 : 과정간의 계의 열역학적 성질이 시간에 따라 변하지 않는 흐름
2)비정상류 : 과정간의 계의 열역학적 성질이 시간에 따라 변하는 흐름
1.5.등류와 비등류
1)등류 : 과정간의 열역학적 성질이 위치에 따라 변하지 않는 흐름
2)비등류 : 과정간의 열역학적 성질이 위치에 따라 변하는 흐름
2.열역학적 성질(상태량)
2.1.점함수(point function)
1)강도성질 : 질량과 무관한 성질 (온도 / 압력 / 밀도 등)
2)종량성질 : 질량에 정비례하는 성질 (내부에너지 / 엔탈피 / 엔트로피 / 체적)
3)비상태량 : 단위질량당의 종량성질 (비체적 / 비엔탈피 / 비엔트로피 / 비내부에너지)>강도성질처럼 취급
2.2.경로함수:물질이 어느상태에서 다른 상태로 변화할 때 어느 과정을 택하느냐에 따라 값이 변하는 함수(일과 열)
2.3.점함수와 경로함수의 미적분
1)점함수의 미분연산자 : d // 경로함수의 미분연산자 : δ
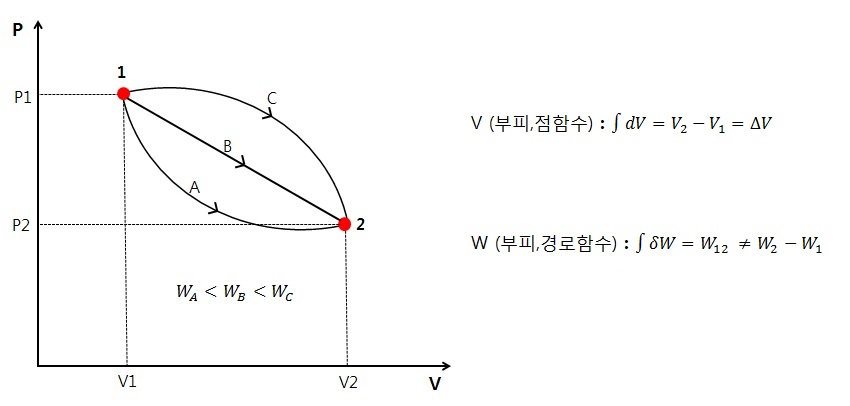
2)다음 그림과 같은 p-v 선도에서 계의 물질이 1번상태에서 2번상태로 변화하는 A,B,C 세가지 경우에 대하여
점함수인 압력과 부피는 1점과 2점에서 일정하지만 과정함수인 일량은 과정에 따라 다르다
3.순환 (cycle)
3.1.순환 : 물질이 한 상태에서 출발하여 여러과정을 거쳐서 원해의 상태로 돌아오는 과정
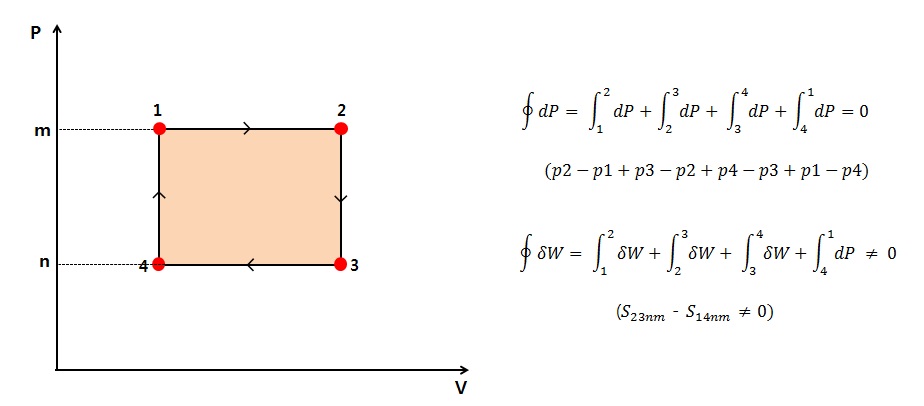
1)한 순환과정에서 점함수의 사이클 적분은 0이다
2)한 순한과정에서 경로함수의 사이클 적분은 0이 아니다
3)다음 그림은 1->2->3->4->1 사이클에서 점함수와 경로함수의 사이클 적분값을 표시한 것이다
4.열역학적 과정
4.1.가역과정과 비가역과정
1)가역과정 : 임의의 과정을 거쳐 다른 상태로 변화한 계가 주위에 아무런 변화도 남기지 않고 원래상태로
돌아갈 수 있는 경우 이를 가역과정이라고 한다 // 이론상으로만 존재하는 과정이다
2)비가역과정 : 가역과정이 아닌 과정을 비가역과정이라한다
4.2.정압/정적/등온/단열 과정 등
1)정압과정 : 압력이 일정한 상태로 변화하는 과정 (P = const // P1 = P2)
2)정적과정 : 부피가 일정한 상태로 변화하는 과정 (V = const // V1 = V2)
3)등온과정 : 온도가 일정한 상태로 변화하는 과정 (T = const // T1 = T2)
4)단열과정 : 계의 열량이 일정한 상태로 변화하는 과정 (S=const//S1=S2//단, 열출입에 의한 엔트로피만 해당)
5)폴리트로픽 과정 : 단열과정에서 몰비열비 대신 폴리트로픽 상수 n 사용//실제기관에 보다 가까운 해석이 가능
5.열평형과 온도
5.1.열평형 : 두 물질의 열 전달이 일어나지 않는 다면 두 물질은 열평형 상태에 있다고 한다
1)열역학 제0법칙 : 계A 와 계B가 열평형이고 계 계B와 계C가 열평형이면 계 A와 계C는 열평형 상태이다
2)열이 높은곳에서 낮은곳으로 이동하는 것은 막을 수 없다 // 결국 어떠한 계는 열평형 상태로 변한다
5.2.온도 : 뜨겁고 차가운 정도를 나타내는 물리량
1)분자운동론에서의 온도 : 분자의 운동에너지에 비례하는 물질 (온도가 높을수록 분자의 운동이 활발하다)
2)섭씨온도와 화씨온도 : 물의 어는점과 끓는점을 기준으로 한 온도단위계
1.섭씨온도 : 물의 어는점을 0℃, 끓는점을 100℃로 하고 그사이를 100등분 한 온도단위계 // 단위 : ℃
2.화씨온도 : 물의 어는점을 32℉, 끓는점을 212℉로 하고 그사이를 180등분한 온도단위계 // 단위 : ℉
3.섭씨온도와 화씨온도의 전환 : ℉ = (℃ x 9/5) + 32
3)절대온도 : 이론적인 최저온도 (기체의 부피가 0이되는 온도)인 절대영도를 기준으로 한 온도단위계
1.켈빈온도 : 이론최저온도를 0K 으로 두고 눈금간격은 ℃와 같은 온도단위계 // 0℃ = 273K // 단위 : K(켈빈)
2.랭킨온도 : 이론최저온도를 0R으로 두고 눈금간격은 ℉와 같은 온도단위계 // 0℉ = 460R // 단위 : R(랭킨)
6.열량과 잠열
6.1.열량 Q : 열의 양을 나타내는 물리량 // 단위 : kcal, Btu, Chu, J 등
1)kcal : 킬로그람 칼로리//1kcal는 표준대기압 하에서 순수한 물 1kg을 14.5℃ 에서 15.5℃로
높이는 데 필요한 열량
2)Btu : British Thermal Unit // 1Btu은 표준대기안 하에서 순수한 물 1lb를 32℉에서 212℉까지
올리는데 필요한 열량의 1/180이다.
6.2.잠열 : 열을 가해도 온도가 변화하지 않는 구간에서 가해지는 열
1)잠열구역 : 열을 가하거나 감하더라고 온도변화가 없는 구역
2)물질의 상태가 변할 때 에너지를 흡수하거나 방출하기 때문에 잠열구역이 발생한다
3)즉 잠열은 물질의 상태변화에 필요한 열에너지라고 할 수 있다
'Aviation > Dynamics' 카테고리의 다른 글
| [열역학 6] 엔트로피의 계산과 무효에너지 (0) | 2023.07.15 |
|---|---|
| [열역학 5] 열역학 법칙과 카르노기관 (0) | 2023.07.15 |
| [열역학 4] 이상기체의 상태변화 (0) | 2023.07.15 |
| [열역학 3] 열역학 제1법칙과 이상기체상태방정식 (0) | 2023.07.15 |
| [열역학 2] 비열/열평형/열효율/일 등 (0) | 2023.07.15 |