1.열용량 / 비열 / 열량
1.2.비열 = (열용량 / 질량) = (열량 / 질량 x 온도차) => c = C/m = Q/mΔT
1)단위질량을 단위온도만큼 올리는데 필요한 열량
2)물의비열 : 1kcal/kg℃ = 4.1855J/gK = 4.1855kJ/kgK // 물의 비열은 물체 중에서 가장크다
1.3.열용량 = (질량 x 비열) = (열량 / 온도차) => C = cm = Q/ΔT // 단위 : kcal/℃, kJ/℃ 등
1.4.열량 = (비열 x 질량 x 온도차) => Q = cmΔT // 단위 : cal, kcal, J, kJ 등
2.열평형과 열역학 제 0법칙
2.1.열역학적 평형 : 온도가 같고 화학적조성도 같으면 기계적으로 평형일 때 열역학적 평형이라 한다
2.2.열역학 제 0법칙 : 어떤 물체 C가 두 물체 A,B와 각각 열평형이면 두물체 A와B도 서로 열평형이다
cf. 열평형과 열역학적 평형은 다른의미 // 열평형 : 온도가 같은 상태
3.열량보존법칙과 열평형온도
3.1.열평형온도 : 고온물체에서 저온물체를 맞닿아 놓으면 고온물체엣 저온물체로 열이 이동하게 된다. 시간이
지나면 두물체는 온도가 같아져 열평형상태가 되고, 이때의 온도를 열평형온도라고 한다
3.2.열량보존법칙 : 고온물체가 잃은 열량과 저온물체가 얻은 열량은 같다
3.3.열량보존법칙으로 열평형온도 구하기 : 고온물체가 잃은 열량Q1 = 저온물체가 얻은 열량 Q2를 이용


4.열효율
4.1.열효율 ηth = 동력 / (저위발열량x연료소비율) = P[kW] / H[kJ/kg] m'[kg/s] => ηth = P/Hm'
4.2.저위발열량과 고위발열량
1)저위발열량 : 연소생성물인 H2O가 기체상태일때의 발열량
2)고위발열량 : 연소생성물인 H2O가 액체상태일때의 발열량
3)응축잠열 : 기체상태의 H2O(수증기)가 물로 응축하면서 외부로 방출하는 열량
4)고위발열량 : 저위발열량 + 응축잠열
5.열전도
1)열전도 : 열의 전달방법(전도/대류/복사)중 하나로 열이 고체매체를 통해 전달되는 방법
2)전도열량 Q는 접촉단면적,온도차,시간에 비례하고 길이(두께)에 반비례함
3)전도열량 Q = KS(T1-T2)t / L (K:열전도율[kJ/m*K*sec or cal/cm*℃*min] S:접촉단면적 t:시간 L:길이)
6.절대일과 공업일
6.1.절대일 (팽창일 / 비유동일 / 밀폐계의 일)
1)P-V선도에서 그래프아래의 면적
2)절대일의 기호 : W (단위질량당의 절대일 : w)
3)절대일의 단위 : J 또는 kJ
4)미소일량 δW = PdV

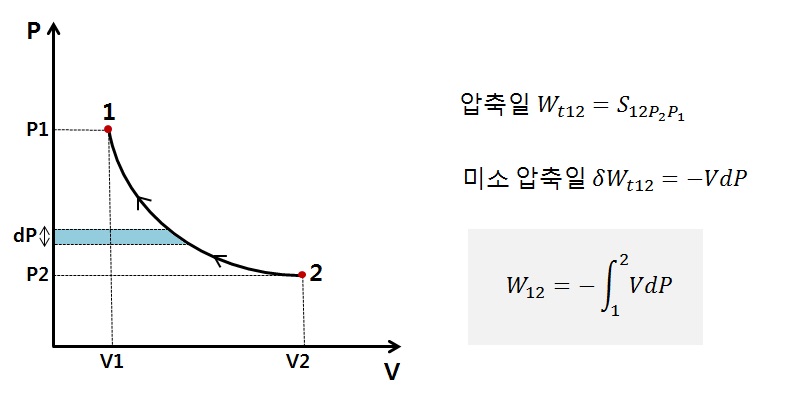
6.2.공업일 (압축일 / 유동일 / 터빈일)
1)V-P선도에서 그래프 아래의 면적
2)공업일의 기호 : Wt (단위질량당의 공업일 : wt)
3)공업일의 단위는 절대일과 동일 (J 또는 kJ)
4)미소일량 δW = -VdP
cf.계의 입장에서 생각하여 계가 일을하는 것(팽창)은 (+)로, 계가 일을받는 것(압축)은 (-)로 한다
'Dynamics & Math > Thermodynamics' 카테고리의 다른 글
| [열역학 6] 엔트로피의 계산과 무효에너지 (0) | 2023.07.15 |
|---|---|
| [열역학 5] 열역학 법칙과 카르노기관 (0) | 2023.07.15 |
| [열역학 4] 이상기체의 상태변화 (0) | 2023.07.15 |
| [열역학 3] 열역학 제1법칙과 이상기체상태방정식 (0) | 2023.07.15 |
| [열역학 1] 계와 기본용어 등 (0) | 2023.07.15 |



